



Fructus Akebiae (FA), suchy owoc Akebia quinata jest powszechnie stosowany jako środek przeciwnowotworowy i moczopędny i oficjalnie udokumentowany w Farmakopei Chińskiej pod nazwą „Yu Zhi Zi”. Badania farmakologiczne wykazały, że ekstrakt z FA posiada silne właściwości przeciwdepresyjne. Uważa się, że glikozydy triterpenowe z hederageniną są głównymi aktywnymi składnikami chemicznymi.
Historia hodowli i udomowienia A. quinata jest krótka; jednak wyhodowano i rozwinięto kilka odmian. Cechy ozdobne, takie jak określony kolor kwiatów lub liści, można wybrać do późniejszej hodowli selektywnej. Na przykład A. quinata „Alba” to odmiana o jasnozielonych łodygach i małych białych kwiatach, z liśćmi, które jesienią stają się jasnożółte. Podobnie A. quinata „Shiro Bana” ma jasnożółte do białych kwiaty, duże żółto-zielone liście i ciemnofioletowe owoce; A. quinata „Silver Bells” ma kremowobiałe kwiaty męskie z ciemnofioletowymi pręcikami i różowymi kwiatami żeńskimi. Akebia quinata „Rosea” ma fioletowo-różowe kwiaty, które są jaśniejsze niż zwykle obserwowane, co jest korzystne, ponieważ zapewnia kontrast z ciemnozielonymi liśćmi, w których występuje. Akebia quinata „Variegata” to wyjątkowa odmiana gatunku z biało-zielonymi plamami na liściach, która stanowi atrakcyjne tło dla różowo-fioletowych kwiatostanów. Wszystkie powyższe odmiany zostały opracowane i uprawiane w ciepłych warunkach.
Akebia quinata została po raz pierwszy opisana w 1779 roku przez Maartena Houttuyna, holenderskiego przyrodnika. Zielnik został zebrany w Japonii i pierwotnie nazwany Rajania quinata. Nazwa A. quinata została oficjalnie opisana w 1845 roku, a gatunek ten został zidentyfikowany jako generytyp rodzaju Akebia. Akebia quinata (nazwa zwyczajowa: pnącze czekoladowe lub pięciolistna Akebia) to pnącze drzewiaste pnące liściaste. Liść złożony tego gatunku jest niebiesko-zielony z pięcioma listkami. Gatunek jest jednopienny, a każdy kwiatostan składa się z jednego lub dwóch kwiatów żeńskich (o średnicy 2,5 cm) i od czterech do dziesięciu kwiatów męskich. Kwiaty żeńskie (ciemnofioletowe) są dwa razy większe niż kwiaty męskie (jasnoróżowe z różowo-fioletowymi pręcikami). Oba kwiaty mają słodki zapach, ale nie zawierają nektaru, nie ma płatków, a działki (od białego do jasnofioletowego) służą do przyciągania zapylaczy. Obserwowana nielosowość w doborze kwiatów przez zapylacze może zwiększać prawdopodobieństwo zapylenia krzyżowego i zmniejszać ryzyko zapylenia geitonogamicznego ze względu na kwiatowy dymorfizm płciowy. Kwitnie od kwietnia do maja, a kwiaty żeńskie otwierają się w kwiatostanie kilka dni wcześniej niż kwiaty męskie. Jednak kwitnienie kwiatów męskich i żeńskich nakłada się w kwiatostanach, co sugeruje, że samozapylenie jest nadal możliwe, podczas gdy wykazano, że samozapylenie geitonogamiczne znacznie zmniejsza produkcję niekrzyżowanych nasion. Owoc Akebia quinata jest mięsistym pęcherzykiem, purpurowym w wieku dojrzałym, prostym lub lekko zakrzywionym i podłużnym do elipsoidalnego kształtu, o średnicy około 3-4 cm i długości 5-8 cm. Każdy owoc ma ponad 100 brązowych do czarnych błyszczących nasion o jajowatym, podłużnym kształcie i jadalnym białym miąższu. Naturalne rozmieszczenie A. quinata obejmuje górskie zbocza na wysokości od 300 do 1500 m w Chinach, na Półwyspie Koreańskim i Japonii. Selekcja siedliskowa na ogół obejmuje ekotony leśne wzdłuż strumieni lub zarośla na zboczach gór, a gatunek generalnie preferuje gleby żyzne i wystarczająco wilgotne, które zapewniają odporność na zimno.
Hederagenina jest saponiną znajdującą się w wielu tradycyjnych lekach i produktach spożywczych i jest badana pod kątem jej możliwych korzyści, ponieważ wiele innych saponin o podobnej strukturze (na przykład kwas ursolowy i kwas korozolowy) zostało odnotowanych jako aktywne biologicznie, jak również znaleźć w różnych produktach spożywczych.
Hederageninę można znaleźć w:
Hedera helix skąd wywodzi swoją nazwę
Chenopodium quinoa (produkt spożywczy znany jako Quinoa) w kwiatach, owocach, nasionach (porcja jadalna przy 27-28% całkowitej zawartości saponin lub 307,8-465 mg na 100 g suchej masy, w tym wszystkie glikozydy) i okrywy nasiennej.
Fructus Akebiae (owoce z rodzaju akebiae, zwykle quinata, nazwa tradycyjnej medycyny chińskiej Ba Yue Zha)
Hederagenina jest tak zwana aglikonem (bez cukru), a inne cząsteczki są znane jako glikony hederageniny, w których cząsteczki cukru są połączone ze strukturą. Glikony te mogą przekazywać organizmowi hederageninę po trawieniu/hydrolizie w celu usunięcia cząsteczki cukru ze struktury, a niektóre z tych glikonów obejmują:
Alfa-Hederyna (Hedera helisa)
Hederakozyd C (Hedera helix)
Asperosaponina IV (z Dipsacus asper), która jest metabolizowana do hederageniny u szczurów, przypuszczalnie przez mikroflorę jelitową
SMG-1 (z Sapindus mukorossi Gaertn)
Glikozyd β-D-glukozylo(1 3)-β-D-galaktozydowy (Quinoa)
Glikozyd α-L-arabinozydowy (Quinoa)
Glikozyd kwasu β-D-glukuronowego (Quinoa)
Glikozyd β-D-glukozylo(1 3)-α-L-ararabinozydowy (Quinoa)
3-O-{β-d-glukopiranozylo-(1→3)-α-l-arabinopiranozylo}-28-O-β-d-glukopiranozyd (Quinoa)
A 3-O-{β-d-glukopiranozylo-(1→4)-β-d-glukopiranozylo-(1→4)-β-d-glukopiranozylo}-28-O-β-d-glukopiranozyd (quinoa)
1. SUROWICA
Odnotowano, że doustna dawka ekstraktu z fructus Akebiae (400 mg/kg, zawierająca 280 mg/kg hederageniny) szczurom zwiększa stężenie w osoczu w ciągu pięciu minut i osiąga szczytowe poziomy 47,73 ng/ml po 20 minutach (oficjalny Tmax 18,33+/- 2,58 m) z 44-minutowym okresem półtrwania.
2. KINETYKA NEURONALNA
Po doustnym spożyciu 280 mg/mg hederageniny (z ekstraktu z owoców Akebiae), które osiągnęło stężenie w osoczu 47,73 ng/ml po 20 minutach, hederageninę wykryto również w płynie mózgowo-rdzeniowym w stężeniu 6,17 +/- 0,22 ng/ml, co sugeruje, że może przenikać bariera krew-mózg.
3. ELIMINACJA
Hederagenina po doustnym podaniu szczurom w dawce 280 mg/kg ma klirens 128,36 ± 9,90 l/m/kg przy stałej eliminacji (Ke) 0,016 ± 0,001 min.
Hederagenina może zwiększać 5-HT, NE i DA w korze czołowej.
Powinowactwo wiązania (jako Ki):
SERT w korze mózgowej: 3,89±0,18 nm
NET w podwzgórzu: 0,22±0,04 nm
DAT w prążkowiu: 2,87 ± 0,54 nm
HG wykazał, że znaczny wzrost poziomu noradrenaliny i serotoniny wykazywał tendencję do zwiększania ekspresji mRNA receptora 5-hydroksytryptaminy (serotoniny) 1A oraz do znacznego zmniejszania ekspresji mRNA dla transportera serotoniny (5-HTT).
W przypadku raka hedaragnina indukuje apoptozę komórek nowotworowych poprzez szlak mitochondrialny.
Hederagenina lub hederyna prowadzą do zmniejszonej fosforylacji p70S6K, która jest dalszym celem mTOR.
SMG-1 hamował wiązanie FMLP ze swoim receptorem w sposób zależny od stężenia... SMG-1 osłabiał indukowany przez FMLP wzrost stężenia wapnia w cytozolu i fosforylację p38 MAPK, ERK, JNK i AKT.
1. EFEKT ANTYDEPRESYJNY
Hedaragnina jest nowym potrójnym inhibitorem transporterów monoamin i działa jako inhibitor wychwytu zwrotnego serotoniny (5-HT), norepinefryny (NE) i dopaminy (DA).
Może również zwiększać ekspresję receptora 5-hydroksytryptaminy 1A (5-HT1A).
Hedaragenina może również obniżać poziom hormonów stresu, takich jak hormon adrenokortykotropowy (ACTH) i kortykosteron w surowicy u szczurów narażonych na przewlekły, nieprzewidywalny, łagodny stres.
Behawioralnie może naśladować działanie przeciwdepresyjne escitalopramu u gryzoni.
2. EFEKT PRZECIWNOWOTWOROWY
Hederagenina działa przeciwnowotworowo przeciwko:
Rak piersi
Rak okrężnicy
Rak głowy i szyi (redukuje NRF2/ARE)
Rak Płuc
Inne pochodne hederageniny mogą być skuteczne przeciwko niektórym nowotworom.
Hedaragenina może również nasilać działanie niektórych środków chemioterapeutycznych.
Na przykład, pochodna hedarageniny H6 może odwrócić oporność wielolekową (MDR) przez uwrażliwienie komórek KBV i MCF7/T na paklitaksel i winkrystynę (stymuluje ATPazę P-gp).
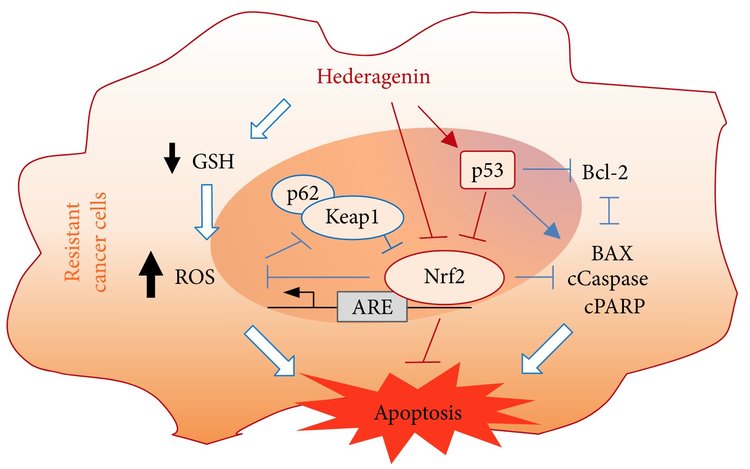
Apoptoza indukowana saponiną hederageniny w różnych typach ludzkich komórek nowotworowych poprzez aktywację składników szlaku apoptozy wewnętrznej, w której pośredniczą mitochondria, takich jak cięta polimeraza poli(ADP-rybozy) (PARP), cięta kaspaza-3, cięta kaspaza-9 i Bax, oraz poprzez hamowanie antyapoptotycznego białka Bcl-2. Natomiast saponina hederageniny nie wpływała istotnie na białka związane z zewnętrznym szlakiem śmierci komórek, takie jak kaspaza-8. Hederagenina została wykorzystana jako szablon triterpenowy do odkrycia nowych związków przeciwnowotworowych. Chociaż te odkrycia sugerują, że w przeciwnowotworowej aktywności hederageniny pośredniczy wewnętrzny szlak śmierci komórek, inne mechanizmy leżące u podstaw śmierci komórek rakowych za pośrednictwem hederageniny nie zostały jeszcze wyjaśnione. Przeciwnowotworowe działanie hederageniny badano w komórkach raka płuc, żołądka, okrężnicy i piersi, ale nie w komórkach HNC. Skuteczność hederageniny in vitro i in vivo powinna być dokładniej zbadana w innych typach raka u ludzi, szczególnie tych, które wykazują oporność na obecne terapie przeciwnowotworowe. Hederagenina skutecznie indukowała apoptozę w komórkach HNC opornych na cisplatynę in vitro i in vivo poprzez celowanie w szlak antyoksydacyjny Nrf2-ARE.
3. CHOROBA HUNTINGTONA I PARKINSONA
Patologie choroby Parkinsona (PD) i Huntingtona (HD) zawierają agregaty białkowe i ciała inkluzyjne (patrz proteopatia).
Hederagenina może poprawić deficyty motoryczne w modelach myszy z chorobą Parkinsona.
Może również promować autofagię i zapobiegać tworzeniu α-synukleiny i huntingtyny (poprzez AMPK-mTOR).
4. DZIAŁANIE OCHRONNE PRZY EKSPOZYCJI NA ALKOHOL
Hederagenina może chronić przed uszkodzeniem wątroby wywołanym alkoholem.
Na przykład w modelach gryzoni hedaragenina była w stanie zmniejszyć stan zapalny związany z używaniem alkoholu i poprawić metabolizm alkoholu.
5. DZIAŁANIE PRZECIWDROBNOUSTROJOWE
Hederagenina działa antybakteryjnie na:
B. cereus
E. coli
E. faecalis
K. pneumoniae
P. aeruginosa
S. aureus
S. epidermidis
S. typhimurium
Hederagenina działa przeciwpasożytniczo na Leishmania infantum
6. DZIAŁANIE PRZECIWZAPALNE
Hederagenina może zmniejszać reakcje zapalne.
Na przykład, leczenie hederageniną może hamować poziomy ekspresji białek stymulowanych lipopolisacharydami iNOS, COX-2 i NF-κB, jak również wytwarzanie NO, PGE2, TNF-α, IL-1β i IL-6.
Hederagenina może również powodować degranulację komórek tucznych.
Saponina hederageninowa SMG-1 jest naturalnym inhibitorem receptora FMLP, który hamuje aktywację ludzkich granulocytów obojętnochłonnych.
7. WPŁYW NA UKŁAD NACZYNIOWY
Hederagenina wykazuje liczne działania farmakologiczne w leczeniu hiperlipidemii, agregacji przeciwpłytkowej i miażdżycy.
Na przykład hederagenina może korygować nierównowagę funkcji śródbłonka poprzez hamowanie uwalniania dużych ilości iNOS i zwiększanie zawartości eNOS oraz hamuje szlak sygnałowy IKKβ/NF-κB w celu zmniejszenia uwalniania IL-6, IFN-γ, TNF-α i inne czynniki zapalne
8. DZIAŁANIE ANTYOKSYDACYJNE
Pochodne hederageniny mogą działać jako wymiatacze wolnych rodników.
Wyciąg z fructus akebiae zawierający wagowo 90% hederageniny nie wydaje się mieć żadnego powinowactwa do receptorów adenozynergicznych A1 ani A2A w stężeniach do 10 μM.
Ekstrakt z fructus akebiae zawierający 90% hederageniny wagowo wykazuje powinowactwo do ludzkiego transportera serotoniny przy Ki 0,65 +/- 0,04 nM (silniejsze niż referencyjna fluoksetyna), konkurując z ligandem citalopramem i zaburzając wychwyt serotoniny.
Wydaje się, że hederagenina nie wchodzi w interakcje z żadnym testowanym receptorem serotoniny w stężeniach do 10 μM.
WNIOSEK: In vitro hederagenina wydaje się być dość silnym inhibitorem wychwytu zwrotnego serotoniny, silniejszym niż fluoksetyna na poziomie komórkowym
Przyjmowanie doustne 12,5-25 mg/kg ekstraktu etanolowego z fructus akebiae (90% hederageniny) u szczurów wydaje się zwiększać stężenie serotoniny w korze czołowej w zależności od czasu i dawki, osiągając maksimum po godzinie i pozostając podwyższone do czterech godzin później.
Ekstrakt z fructus akebiae zawierający 90% hederageniny wagowo wykazuje powinowactwo do transportera dopaminy przy Ki 1,03 +/-0,04 nM (silniejsze niż nomifensyna referencyjna) i zapobiega wychwytowi dopaminy.
Ten sam ekstrakt nie wszedł w interakcję z żadnym testowanym receptorem dopaminy (D1 do D5) do 10 μM
WNIOSEK: Wydaje się, że hederagenina jest inhibitorem wychwytu dopaminy, aktywnym w stężeniach porównywalnych do tego, gdy jest aktywny zarówno na wychwyt serotoniny, jak i noradrenaliny
Przyjmowanie doustne 12,5-25 mg/kg ekstraktu etanolowego fructus akebiae (90% hederageniny) u szczurów wydaje się zwiększać zależnie od czasu i dawki stężenia dopaminy w korze czołowej, osiągając szczyt po godzinie i pozostając powyżej poziomu wyjściowego cztery godziny później.
WNIOSEK: Połknięcie doustne hederageniny wydaje się zwiększać stężenie dopaminy w korze czołowej szczurów po podaniu pojedynczej dawki
Ekstrakt z fructus akebiae zawierający 90% hederageniny wagowo wykazuje powinowactwo do transportera noradrenaliny o wartości Ki 140 pM (silniejsze niż dezypramina referencyjna) i konkuruje z ligandem nisoksetyną oraz hamuje wychwyt noradrenaliny in vitro.
Ekstrakt ten nie wydaje się wpływać na żaden receptor adrenergiczny testowany w tkance nerwowej (receptory alfa i β1) i podczas gdy glikon hederageniny (α-hederyna) wydaje się zwiększać wiązanie ligandu β2 i aktywność receptora związaną z mniejszą internalizacją receptora w w zakresie 2-50 nM ta właściwość nie rozciąga się na czystą hederageninę.
WNIOSEK: Wydaje się, że hederagenina zapobiega wchłanianiu noradrenaliny o sile silniejszej niż dezypramina i nie wydaje się mieć żadnego znanego powinowactwa do receptorów adrenaliny
Doustne przyjmowanie 6,25-25 mg/kg ekstraktu etanolowego z fructus akebiae (90% hederageniny) u szczurów wydaje się zwiększać zależnie od czasu i dawki stężenie noradrenaliny w korze czołowej, osiągając maksimum po jednej godzinie i pozostając podwyższone do czterech godzin.
WNIOSEK: Doustne przyjmowanie nawet niskich dawek hederageniny wydaje się zwiększać noradrenalinę w korze czołowej szczurów po pojedynczej dawce
Podczas testowania w stężeniach do 10 μM ekstrakt z fructus akebiae zawierający 90% hederageniny nie wszedł w interakcję z żadnym receptorem muskarynowym acetylocholiny (M1 do M5).
WNIOSEK: Wydaje się, że hederagenina nie wykazuje żadnego znanego powinowactwa do muskarynowych receptorów acetylocholiny, brak danych na temat receptorów nikotynowych
Hederagenina (poprzez ekstrakt z fructus akebiae, który stanowił 90% hederageniny w masie) nie wydaje się oddziaływać z żadnym testowanym receptorem histaminowym w stężeniach do 10 μM.
WNIOSEK: Wydaje się, że hederagenina nie wykazuje powinowactwa do receptorów histaminowych w stężeniu kilkakrotnie wyższym niż jego działanie na inne mechanizmy
Ekstrakt z fructus akebiae zawierający 90% hederageniny wagowo nie wszedł w interakcję z żadnym podzbiorem receptorów opioidowych (μ, κ lub δ) w stężeniach do 10 μM in vitro
WNIOSEK: Stężenia hederageniny, które są aktywne w mózgu na inne mechanizmy, nie wydają się wywierać wpływu na neuroprzekaźnictwo opioidergiczne, ponieważ nie jest znane powinowactwo do receptorów
Powyższe badania mają charakter typowo informacyjny oraz były wykonawane z udziałem róznych ekstraktów, innych niż dostępny w ofercie sklepu. Dlatego też nie można ich traktować jako wiarygodne źródło informacji na temat produktu dostępnego w naszej sprzedaży oraz sugestię co do jego spożywania. Informacje zawarte w opisach nie są zatwierdzone przez GIF, GIS oraz EFSA i nie mają na celu leczenia, diagnozowania lub zapobiegania jakiejkolwiek chorobie.
Ten produkt nie jest suplementem diety na terenie Polski. Informacje zawarte w opisach nie są zatwierdzone przez GIF, GIS oraz EFSA i nie mają na celu leczenia, diagnozowania lub zapobiegania jakiejkolwiek chorobie.
Cytowane badania naukowe nie mogą być uważane za jednoznaczne z uwagi na ich ograniczony charakter i nie muszą ujawniać pełnego spektrum działania substancji.
Opinie klientów zawarte w kartach produktów nie są opiniami ekstrakty.com oraz nie mogą być uznawane za zalecenia do ich stosowania. Ekstrakty.com nie bierze odpowiedzialności za informacje w nich zawarte.
Zawsze skonsultuj się z lekarzem lub farmaceutą podczas stosowania nowego środka nootropowego. Obsługujemy tylko osoby pełnoletnie i nie bierzemy odpowiedzialności za niewłaściwe stosowanie zakupionych produktów.
Dokładamy wszelkich starań by opis właściwości, działanie, dawkowanie, zastosowanie produktów oraz cena były wykonane możliwie rzetelnie i precyzyjnie. Nasz sklep to nie apteka, dzięki czemu masz prawo do zwrotu nieotwartego produktu bez podania przyczyny w ciągu 30 dni.
Zaloguj sie